Forschungsbericht 2020 - Max-Planck-Institut für Kolloid- und Grenzflächenforschung
Kohlenhydrate unter dem Mikroskop
Kohlenhydrate – auch bekannt als Zucker – machen fast 80 Prozent der natürlichen Biomasse aus und sind dadurch eine attraktive Quelle für erneuerbare und biokompatible Materialien. Sowohl in der Biologie und den biomedizinischen Wissenschaften (zum Beispiel Nanomaterialien für Tissue Engineering und Zellwachstum) als auch in der industriellen Massenproduktion ( zum Beispiel Papier- und Textilindustrie) gibt es vielfältige Anwendungen dieser Verbindungsklasse. Die Nutzung von Kohlenhydraten beziehungsweise Polysacchariden ist jedoch auch mit einigen Problemen verbunden. Diese Substanzen aus natürlichen Quellen zu gewinnen , ist schwierig und resultiert in heterogenen Proben; das erschwert die Analyse, Reproduzierbarkeit und Qualitätskontrolle.
Chemische Modifikationen von Kohlehydraten zur Kontrolle ihrer physikalischen und mechanischen Eigenschaften sind nicht selektiv; dadurch erhöht sich ihre Heterogenität noch weiter. Deswegen sind die Korrelationen zwischen der Struktur und Funktion dieser Materialklasse weitgehend unbekannt. Das Verständnis von Kohlenhydraten auf molekularer Ebene ist der Schlüssel dazu, ihr Potenzial voll auszuschöpfen. Kontrollierte Modifikationen sind für biologische Experimente, bei denen eine hohe Reproduzierbarkeit von Charge zu Charge und eine Qualitätskontrolle unerlässlich sind, von entscheidender Bedeutung. Aufgrund der enormen Komplexität von Kohlenhydraten ist deren Bedeutung im Vergleich zu anderen Biomolekülen (zum Beispiel Peptiden) gering.
Definierte Kohlenhydrate

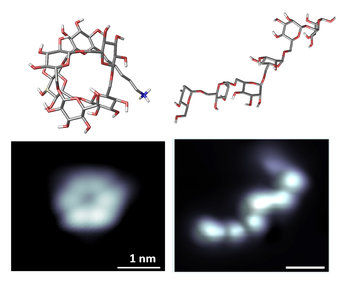
Abb. 1: Kohlenhydrate nehmen je nach ihrer chemischen Zusammensetzung unterschiedliche Konformationen ein, die mittels Molekulardynamik-Simulationen (oben) und Einzelmolekül-Bildgebung (unten) untersucht werden.
Wir nutzen spezielle Methoden, wie die automatisierte Festphasenglykansynthese („Automated Glycan Assembly“, AGA), um in relativ kurzer Zeit definierte Polysaccharide in hoher Reinheit herzustellen. Auf diese Weise können wir beispielsweise die Länge und Modifikation dieser Biopolymere kontrolliere und deren Einfluss auf die molekularen Eigenschaften studieren. Um die räumliche Struktur von Polysacchariden zu untersuchen, setzen wir spezielle analytische Methoden wie Computersimulationen, NMR-Spektroskopie und spezielle Bildgebungstechniken für Einzelmolekülexperimente (single molecule imaging) ein. Dabei entdeckten wir, dass einige Polysaccharide Helices bilden, während andere stäbchenförmige Strukturen annehmen (Abbildung 1). Indem wir die Zuckerkette an bestimmten Positionen chemisch modifizieren, können wir die dreidimensionalen Strukturen solcher Verbindungen und die damit verbundenen Eigenschaften (zum Beispiel die Löslichkeit) kontrollieren.[1] Basierend auf diesen Erkenntnissen haben wir mehrere unnatürliche Modifikationen entworfen, die selektiv die Form und Aggregation natürlicher Polymere verändern und dadurch einen Werkzeugkasten für die Herstellung von Biomaterialien bereitstellen.[2]
Visualisierung einzelner Moleküle
Ein wichtiger Meilenstein für die strukturelle Charakterisierung von Kohlenhydraten ist die Visualisierung einzelner Moleküle. In Zusammenarbeit mit dem MPI-FKF konnten wir einzelne Glykane mittels Elektrospray(ES)-Abscheidung und Rastertunnelmikroskopie (STM) abbilden.[3] Die Zuckerketten wurden ionisiert, in den gasförmigen Zustand gebracht und als einzelne Moleküle auf einer Kupferoberfläche abgeschieden. Die Oberfläche wurde bei niedriger Temperatur (4,5 Kelvin) mit der Spitze eines Rastertunnelmikroskops abgetastet, um ein Profil des Zuckermoleküls zu erstellen. Mit der ES-STM-Methode konnten wir einzelne Zuckermoleküle in hoher Auflösung sichtbar machen und wiederkehrende Strukturmerkmale identifizieren (siehe Abb. 1). Durch die Abstimmung der Energie der Glykanabscheidung konnten wir die verschiedenen Konformere, die ein bestimmtes Glykan annehmen kann, beobachten.[4]
Kohlenhydrataggregate

Abb. 2: Beispiele für Kohlenhydratmaterialien, die aus synthetischen Oligosacchariden und Kristalleinheiten gewonnen wurden und mittels MikroED-Analyse rekonstruiert wurden.
Da Polysaccharide bevorzugt hierarchische Architekturen mit unterschiedlichen physikalischen Eigenschaften bilden, sind sie äußerst vielversprechend für die Herstellung von speziellen Biomaterialien. Wir fanden heraus, dass einfache synthetische Kohlenhydrate sich selbst zu wohldefinierten Morphologien zusammenfügen, die von kugelförmigen Partikeln bis hin zu Fasern und Gelen reichen (siehe Abb. 2). [5]
Aufgrund ihrer definierten chemischen Zusammensetzungen bieten diese synthetischen Kohlenhydratmaterialien perfekte Modellsysteme, um die Faktoren zu erforschen, die den Kohlenhydrataufbau in der Natur steuern. Mittels Microcrystal Electron Diffraction (MicroED) bei kryogener Temperatur konnten wir die Kristalleinheit sowie die größere supramolekulare Architektur unserer synthetischen Kohlenhydratmaterialien rekonstruieren (siehe Abb. 2). Diese Ergebnisse sind ein erster Schritt zum Verständnis der Kohlenhydrat-Wechselwirkungen in der Natur. Indem wir erforschen, wie sich künstliche Kohlenhydrate zusammenlagern und Materialien erzeugen, können wir herausfinden wie sich neuartige Kohlenhydratmaterialien mit maßgeschneiderten Eigenschaften für medizinische Anwendungen kreieren lassen.
Literaturhinweise
Angew. Chem., Int. Ed. 2020, (10.1002/anie.202008153).