Forschungsbericht 2014 - Max-Planck-Institut für Biologie Tübingen
Das Ubiquitin-Proteasom-System: Strukturelle Einblicke in einen zellulären Protein-Schredder
Einleitung
Kein Lebewesen, sei es nun einzellig oder so komplex wie der menschliche Körper, wäre ohne die Fähigkeit der Zellen, zuverlässig und effizient auf Signale aus der Umwelt zu reagieren, überlebensfähig. Wenn wir uns aufregen, steigt unser Puls und unser Atem beschleunigt sich. Auf zellulärer Ebene wird diese physiologische Reaktion durch die Freisetzung eines kleinen Signalmoleküls verursacht, dem Hormon Adrenalin, das an Rezeptorproteine auf der Zelloberfläche bindet und dadurch auf fast alle Körpergewebe einwirkt. Dieses chemische Signal löst eine Kaskade biomolekularer Wechselwirkungen aus, die von der Zelloberfläche ausgehend Signale an Zielproteine innerhalb der Zelle übertragen. Wie umfallende Dominosteine aktiviert der Rezeptor ein Protein, das wiederum ein weiteres Protein aktiviert usw., um schließlich eine zelluläre Reaktion zu erzeugen. Und genauso, wie wir uns nach einer Aufregung beruhigen, kehren die Zellen in einen inaktiven Zustand zurück.
Eine der Strategien, zelluläre Signalprozesse zu beenden, besteht darin, die beteiligten Komponenten abzubauen. Ohne die Beendigung würden die Zellen darüber hinaus ihre Reaktionsfähigkeit gegenüber neuen Signalen verlieren. Zudem führen nicht richtig beendete Signalprozesse zu schwerwiegenden zellulären Dysfunktionen, die zahlreiche menschliche Krankheiten verursachen. So ist beispielsweise auch Krebs das Ergebnis eines unkontrollierten Zellwachstums aufgrund von Zellen, die ihre Fähigkeit zur Inaktivierung bestimmter Signalübertragungswege verloren haben.
Das Ubiquitin-Proteasom-System

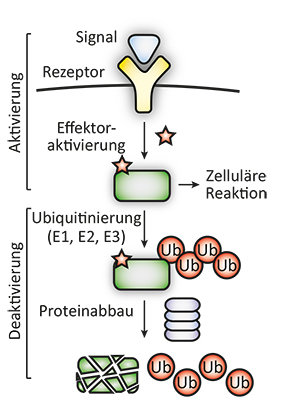
Damit nicht mehr benötigte oder in der Zelle fehlplatzierte Proteine entfernt werden können, wird den Zielproteinen ein molekularer Stempel – Ubiquitin – angehängt, um sie für den Abbau zu markieren (Abb. 1; [1, 2]).
Die zelluläre Maschinerie, die diese Protein-Ubiquitinierung katalysiert, besteht aus drei Enzymen: einem Ubiquitin-aktivierenden Enzym (E1), einem Ubiquitin-konjugierenden Enzym (E2) und einer Ubiquitin-Ligase (E3; Abb. 2). Das menschliche Genom kodiert zwei E1-Enzyme, etwa fünfzig E2-Enzyme und hunderte E3-Enzyme. Die Diversität dieser Enzyme und die enorme Anzahl möglicher E2-E3-Kombinationen repräsentiert die große Bandbreite von Zielproteinen und regulierenden Mechanismen, an denen Ubiquitinierungsenzyme beteiligt sind. Schließlich werden die ubiquitinierten Proteine in der Zelle von einem sogenannten Proteasom, einer zylinderförmigen Struktur, die Proteine in kleine Peptid-Einheiten abbaut, erkannt.
Welche Enzyme für die Markierung von Proteinen mit Ubiquitin verantwortlich sind, ist weitestgehend bekannt. Wir sind aber noch weit davon entfernt zu verstehen, wie Ubiquitinierungsenzyme auf atomarer Ebene funktionieren und wie ihre Funktion und Aktivität reguliert wird. Das Ziel unserer Forschungsaktivitäten besteht darin, die der Ubiquitinierungsreaktion zugrunde liegenden molekularen Mechanismen aufzuklären. Dazu bestimmen wir die dreidimensionalen Strukturen von Ubiquitinierungsenzymen mit atomarer Auflösung mit Hilfe einer Technik, die als NMR-Spektroskopie (Nuclear Magnetic Resonance) bezeichnet wird. In Kombination mit funktionellen Assays ermöglicht uns dies, zu verstehen, wie diese Proteine ihre jeweiligen Aufgaben in der Zelle erfüllen und wie Defekte in der dreidimensionalen Struktur des Proteins zelluläre Fehlfunktionen und Krankheiten verursachen können.

Die Leistungsfähigkeit der NMR-Spektroskopie nutzen
Die NMR-Spektroskopie ist eine biophysikalische Methode, die sich eine als Spin bezeichnete Eigenschaft bestimmter Atomkerne (z.B. 1H, 13C und 15N) zunutze macht. Werden diese Atome in ein starkes Magnetfeld gebracht, resonieren sie mit einer sogenannten Spin-Frequenz, die für jedes Atom in einem Protein einzigartig ist. Die Resonanzfrequenz hängt von der chemischen Umgebung eines jeden Atoms ab und liefert deshalb Informationen über die räumliche Anordnung der Atome im Protein. Aus NMR-Daten können die dreidimensionalen Strukturen von Proteinen ermittelt werden und wie die Proteine miteinander interagieren.
NMR-Untersuchungen großer Proteine sind jedoch aufgrund der zunehmenden Anzahl von Atomen im Protein äußerst kompliziert und erfordern spezielle Techniken. Eine davon nutzt die Methylgruppen in Protein-Seitenketten als NMR-Sonden, sie wird daher als Methyl-NMR-Spektroskopie bezeichnet [3]. Mithilfe dieser Techniken können Proteinkomplexe mit Molekulargewichten erforscht werden, die die traditionelle Grenze von rund 50 kD weit überschreiten.
Wir haben eine als Methionin-Scanning bezeichnete Methode entwickelt, die zwei wesentliche Nachteile der methylbasierten NMR-Spektroskopie überwindet [4]: Die potenziell unzureichende Anzahl von Methylsonden an der betreffenden Stelle und das Fehlen von unkomplizierten Methylresonanz-Zuordnungsstrategien. Um diese beiden Probleme zu überwinden, werden an speziellen Stellen mittels Mutagenese Methionin-Reste als Methyl-Reporter in Proteine eingebracht. Dadurch können alle neu entstehenden Resonanzen der Reporter-Methionine direkt zugeordnet und Proteininteraktionsoberflächen auf der Basis jeder einzelnen Aminosäure ermittelt werden (Abb. 3). Darüber hinaus wird die Bedeutung jeder einzelnen Mutation für die Liganden-Bindung untersucht. Durch diesen Ansatz erweitern sich das Anwendungsspektrum, der Informationsinhalt und die räumliche Auflösung von methylbasierten NMR-Experimenten erheblich. Derzeit wird diese Methode intensiv zur Erforschung von Wechselwirkungen innerhalb von Ubiquitin-Ligasen (intramolekular) und E3-Interaktionen mit anderen Proteinen (intermolekular) genutzt, um nachzuvollziehen, wie diese Wechselwirkungen insbesondere die E3-Enzymaktivität regulieren. Zusätzlich wollen wir die Anwendbarkeit dieses Ansatzes auf Systeme mit sehr hohen Molekulargewichten, wie etwa das Proteasom (> 500 kD), etablieren.

Die Inaktivierung von E3-Enzymen
Kürzlich wurde ein Regulationsmechanismus identifiziert, der bestimmte Ubiquitin-ligierende Enzyme - Ligasen des sogenannten HECT-Typs - in einem inaktiven Zustand hält [5]. Erst wenn das richtige Zielprotein erkannt wird, schaltet das Enzym von einer „Aus“ auf eine aktive „An“-Konformation um und stellt so sicher, dass Zielproteine nicht unkontrolliert ubiquitiniert und abgebaut werden. Mit Hilfe unserer Methionin-Scanning-Methode, wie oben erläutert, haben wir nunmehr die strukturelle Basis für die HECT-E3-Enzyminaktivierung aufgeklärt [6]. E3s des HECT-Typs sind eine wichtige Kategorie von Ubiquitin-Ligasen, die durch Schließen einer kovalenten Bindung an Ubiquitin zunächst Ubiquitin vom E2-Enzym übernehmen. Danach wird Ubiquitin vom E3 auf das Zielprotein übertragen. In Kombination mit biochemischen Experimenten haben wir durch unsere NMR-Analysen nachgewiesen, dass eine bestimmte Region innerhalb des E3-Enzyms, die sogenannte C2-Domäne, die katalytische HECT-Domäne auf zwei Ebenen inaktiviert (Abb. 4): Die C2-Domäne verhindert die Ubiquitin-Übertragung vom E2- auf das E3-Enzym. Gleichzeitig beeinträchtigt die C2-Domäne die Bindung des ubiquitinierten Zielproteins an die HECT-Domäne und unterdrückt damit die Prozessivität der Ubiquitinierungsreaktion [6, 7].

Insgesamt liefern diese Untersuchungen wichtige Erkenntnisse über die Funktion von E3-Enzymen und die strukturellen Prinzipien, die der E3-Inaktivierung zugrunde liegen. Letztendlich tragen die gewonnenen Strukturinformationen dazu bei, die unterschiedlichen Regulationmechanismen der E3-Enzyme zu nutzen, um spezifische, pharmazeutische Inhibitoren, beispielsweise zur Behandlung von Krebs, zu entwickeln.
Ubiquitin und Krebsentstehung
Die Dysregulation des Ubiquitin-abhängigen Proteinabbaus wird mit dem Entstehen und Fortschreiten von Krebs und vielen anderen menschlichen Krankheiten in Verbindung gebracht. Somit kristallisiert sich das Ubiquitin-Proteasom-System als eine vielversprechende Kategorie von Zielproteinen für die Arzneimittelentwicklung heraus. Da E3-Enzyme der Ubiquitinierungsreaktion ein hohes Maß an Spezifität und Selektivität verleihen, sind sie inzwischen bevorzugte Ziele in der Wirkstoffentwicklung.
In der Zelle agieren E3-Enzyme wie Drehkreuze, die vielfältige Protein-Protein-Interaktionen organisieren, um deren katalytische Aktivität streng zu regulieren. Wenn auch bereits eine ganze Reihe an Regulationsmechanismen beschrieben wurde – insbesondere die Kooperation mit E2-Enzym(en), die Substraterkennung und die E3-Prozessivität – so ist doch die Vorstellung darüber, wie inter- und intramolekulare Interaktionen die Ubiquitin-Ligase-Aktivität modulieren, noch weitestgehend unvollständig.
Die Analyse der grundlegenden Mechanismen für die Protein-Ubiquitinierung hat umfassende Auswirkungen auf unser Verständnis von fundamentalen biologischen Prozessen und kann zu neuartigen therapeutischen Strategien für die Entwicklung von Biomarkern zur Krankheitserkennung und zu einem modernen, strukturbasierten Rational Drug Design führen.