Forschungsbericht 2023 - Max-Planck-Institut für Festkörperforschung
Vom Zahn der Zeit zernagt: Wie Kristallstrukturanalyse aus Röntgenbeugungsdaten an Pulvern hilft, die „Bynes Krankheit“ zu besiegen
Historische Objekte sind während der Lagerung in Museen und Sammlungen Luftfeuchtigkeit und atmosphärischen Gasen wie Kohlendioxid (CO2) und Sauerstoff (O2) über Jahrhunderte ausgesetzt. Zusätzlich stoßen Holzmöbel und -vitrinen, besonders solche aus Eichenholz, Ameisen- und Essigsäure oder deren Vorstufen aus: Form- und Acetaldehyd. Infolgedessen kommt es zu verschiedenen Korrosionsprozessen, die mitunter beträchtliche Beschädigungen des betroffenen Objekts nach sich ziehen.
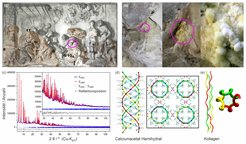
Das Auftreten von weißen, nadelförmigen Ausblühungskristallen auf kalkhaltigen Objekten (Abb. 1(a)–(b), Abb. 2(a)–(e)), auch bekannt als „Bynes Krankheit“, stellt ein bereits Ende des 19. Jahrhunderts bekanntes Problem für Museen und Sammlungen dar. Hierbei handelt es sich um calciumcarboxylathaltige Salze, die entweder die gesamte Oberfläche des Objektes überwachsen oder in Poren und Rissen kristallisieren und somit Kulturgüter enorm schädigen können. Bekannte Vertreter dieser Ausblühungsphasen sind chemisch formuliert: Ca(CH3COO)2·H2O, Ca(CH3COO)2·½H2O [1], Calclacit (Ca(CH3COO)Cl·5H2O), Thecotrichite [2] (Ca3(CH3COO)3Cl(NO3)2·6H2O), Tennents Salz (Ca(CH3COO)(HCOO)·H2O) [3] und Ca2(CH3COO)(HCOO)(NO3)2·4H2O [4].
Da die Ausblühungen an historischen Objekten nie einkristallin auftreten, ist eine Kristallstrukturbestimmung nur durch röntgenographische Analyse des polykristallinen Pulvers möglich (Abb. 1(c)). Signifikante Fortschritte in Hard- und Software während der letzten zwei Dekaden haben es ermöglicht, zuverlässige Strukturdaten auch ohne das Vorhandensein von Einkristallen zu gewinnen. Die Kristallstrukturen aller bekannten Ausblühungsphasen zeigen große Gemeinsamkeiten: Calcium ist in diesen Verbindungen immer von acht Liganden umgeben. Hierbei sind jeweils vier von acht Koordinationsstellen durch Carboxylat-Ionen besetzt, wodurch sich 1-dimensionale Calciumcarboxylatketten bilden (Abb. 1(d), Abb. 2(f)). Auf den übrigen Koordinationsstellen befinden sich Hydratwassermoleküle, Acetat- oder Nitrat-Ionen, wobei die letzten beiden zur Vernetzung der Carboxylatketten untereinander führen können. Weiterhin können im Zwischenraum der Ketten, wie im Fall von Calclacit oder Thecotrichit, Hydratwassermoleküle oder Chlorid-Ionen eingelagert werden. Die Calciumcarboxylatketten verlaufen jedoch nicht bei allen Phasen linear. Überraschenderweise bilden die Carboxylatketten in der Struktur der chemisch scheinbar einfachen Verbindung Ca(CH3COO)2·½H2O ein komplexes, den Kollagenproteinen analoges Tripel-Helix-Motiv aus (Abb. 1(f)).

Neben dem rein wissenschaftlichen Interesse kann die Kristallstrukturaufklärung der Ausblühungsphasen auch Beiträge zum Erhalt der kalkhaltigen Kulturgüter liefern. Die Strukturdatensätze stellen die Grundlage der qualitativen und quantitativen Phasenanalyse mittels Röntgenpulverdiffraktometrie dar. Weiterhin zeigt das Carboxylatkettenmotiv, was allen Strukturen gemeinsam ist (Abb. 1(e)), deutlich auf, dass nur die Carboxylat-Anionen zum Aufbau der Ketten nötig sind und nicht die anorganischen Anionen. Somit wird klar, dass Ausblühungen auch auftreten, nachdem die Objekte aufwendig entsalzt wurden. Die zwischen den Carboxylatketten eingelagerten Wassermoleküle sind nur schwach gebunden und können daher leicht abgespalten werden. Da die wasserhaltigen Ausblühungsphasen ein reversibles Dehydrationsverhalten aufweisen, können Schwankungen in der Lufttemperatur und -feuchte durch den Hydratationsdruck der Calciumacaboxylate zu einer weiteren Schädigung der Objekte führen.













